2024: Warum das Startup, das in den USA Finanzierungsrekorde bricht, "nur" dieses neue chinesische Medikament liebt | Branchenanalyse
Die BD- und NewCo-Szene im Pharmabereich war das ganze Jahr über lebhaft. Gegen Ende Dezember fand schließlich das spannendste "Winner-takes-all"-Ereignis des Jahres statt.
Kürzlich gab das amerikanische "Dark Horse" Candid Therapeutics, ein Innovator im Bereich der Medikamentenentwicklung, gleich drei Transaktionen bezüglich TCE-Produkten bekannt. Der offengelegte Betrag überschreitet 1,3 Milliarden Dollar. Berücksichtigt man die Übernahme von zwei auf TCE fokussierten Innovatoren im September dieses Jahres, hat Candid bereits fünf Zusammenarbeiten in Bezug auf TCE-Produkte abgeschlossen, wobei die Partner allesamt chinesische Unternehmen oder von Chinesen in den USA gegründete Pharmafirmen sind.
Grafik von 36Kr, Datenquelle: Öffentliche Informationen
TCE-Bi-specific Antikörper sind im Grunde eine Art Immuntherapie, die T-Zellen aktivieren kann. Im Vergleich zu den weithin bekannten CAR-T-Produkten, die "eine Million pro Spritze" kosten, sind sie benutzerfreundlicher und kostengünstiger.
Candid wurde mit einem "Star-Glanz" gegründet und erreichte im September mit einer Finanzierungsrunde von 370 Millionen Dollar einen Rekord im Biopharmasektor dieses Jahres. Hinter dem Unternehmen stehen nicht nur fast 20 US-Dollar-Fonds wie Foresite Capital und Venrock Healthcare Capital Partners, sondern auch der Gründer Ken Song, ein in der Branche hoch angesehener und kapitalisierungsfähiger Serienunternehmer. Kurz vor der Gründung von Candid wurde sein Innovationsprojektunternehmen für Medikamente von Bristol-Myers Squibb für 4 Milliarden Dollar übernommen.
Diese Zusammensetzung und die Schnelligkeit des "Einkaufsrausches" sind fast eine öffentliche Erklärung an die globale Pharmabranche, dass Spitzenkapital und Unternehme auf das TCE-Gebiet derzeit so viel Wert legen. Und Candid könnte das wettbewerbsfähigste TCE-Unternehmen der Branche sein.
Es ist bemerkenswert, dass TCE-Asset-Transaktionen auch in diesem Jahr ein heißer BD-Trend waren. Neben Candid haben auch internationale Pharmakonzerne wie GlaxoSmithKline und Merck Vereinbarungen mit chinesischen Innovatoren über TCE-Produkte getroffen. Als Merck die TCE-Linie von ReignBio kaufte, betrug die Anfangszahlung bereits 700 Millionen Dollar.
In den letzten Jahren gab es viele heiße Forschungsrichtungen in der Medizinbranche, doch nur wenige haben solch eine Auszeichnung erhalten.
Angesichts in der Erwartung, dass der Wohlstand in die Pharmaindustrie zurückkehrt, bleibt die Frage, welchen Einfluss das TCE haben wird. Welche Rolle werden chinesische Unternehmen dabei spielen?
2024 – der heißeste neue BD-Trend im Bereich neuer Medikamente
Unterschätze niemals den Wunsch der Wissenschaftler, den neuesten Trend zu verfolgen.
In der Pharmaindustrie sind die Implementierung eines neuen Mechanismus oder Rekordumsätze eines bestimmten Produkttyps oft der Katalysator für einen BD-Boom dieses Produkttyps, wie in der Vergangenheit bei PD-1, ADC und jetzt TCE.
Seit Anfang dieses Jahres ist dies auch der Schwerpunkt der Einkaufsaktivitäten internationaler Pharmaunternehmen in China. Nach unvollständigen Statistiken von 36Kr haben mindestens sieben chinesische Pharmaunternehmen in diesem Jahr ihre TCE-Vermögenswerte internationalisiert, darunter Genor Biopharma, ReignBio, Incyte Biopharma, Vision Medicals, und CanSino Biologics.
Zurück zur zentralen Frage: Was genau sind TCEs?
Aus einer technischen Perspektive handelt es sich um innovative biotechnologische Antikörper mit der Fähigkeit, gleichzeitig zwei unterschiedliche Antigene an zwei verschiedenen Zellen zu binden. Auf einer Seite ist das CD3-Molekül auf der T-Zelle, und auf der anderen ein spezifisches Antigen von Tumorzellen oder Zellen, die mit Autoimmunerkrankungen assoziiert sind. Im Vergleich zu traditionellen monoklonalen Antikörpern sind TCE-Bi-specific-Antikörper so gestaltet, dass sie den Abstand zwischen T-Zellen und Zielzellen verringern, was zur Aktivierung von T-Zellen und damit zu einer stärkeren "Tötungs"-Wirkung führt.
Aufgrund ihrer exprimierbaren Eigenschaften in den meisten Tumorzellen nehmen bi-spezifische Antikörper-Linien, die auf CD3 basieren, fast die Hälfte der Forschungslandschaft für die Entwicklung von Bi-specific-Antikörpern weltweit ein. Aus kommerzieller Sicht bieten TCE-Produkte darüber hinaus erhebliche Kostenvorteile und Sicherheitsgewinne.
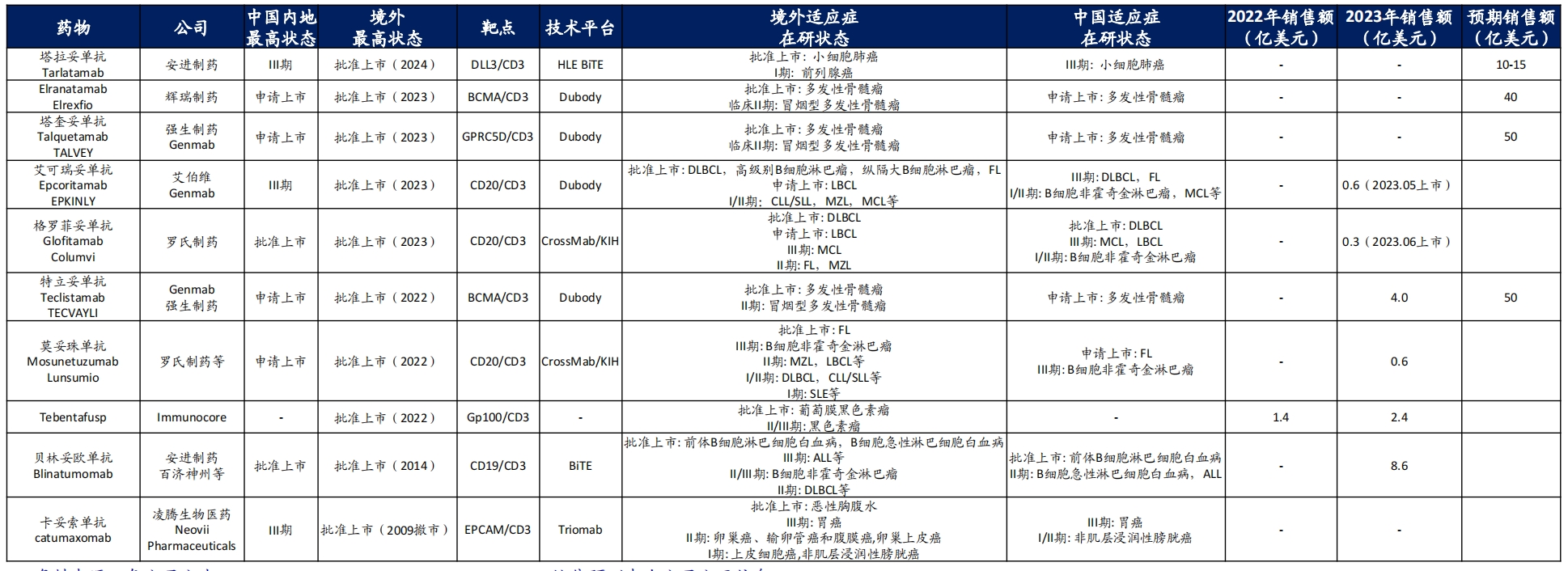
In frühen Jahren war der TCE-Markt im Fokus internationaler Pharmaunternehmen. Bis heute sind weltweit 11 TCE-Medikamente zugelassen, mit häufigen Target-Kombinationen wie CD3×CD19, CD3×CD20, CD3×BCMA, die in der Behandlung von Blutkrebs wie Multiplem Myelom und diffusen großen B-Zell-Lymphomen eingesetzt werden.
Zugelassene TCE-Produkte (Bildquelle: Haitong International Research Report)
In Vertriebsfragen haben einige TCE-Produkte bereits "Blockbuster"-Material gezeigt. So hat beispielsweise Johnson & Johnson Prognosen für zwei ihrer Produkte auf 5 Milliarden Dollar angehoben.
Unter dem Druck eines großen Marktes sind auch chinesische Pharmaunternehmen entschlossen, ein Stück vom "Kuchen" zu sichern. Laut Haitong Securities gibt es derzeit allein in den Bereichen Hämatomen und soliden Tumoren 30 laufende klinische Projekte für TCE-Bi-specific Antikörper in China.
Im Vergleich dazu haben chinesische Unternehmen jedoch einerseits mit einem späteren Start in der Entwicklung bi-spezifischer Antikörper zu kämpfen, andererseits stellen bestehende, ausgereifte Produkte in relativ einfach zu behandelnden hämatologischen Indikationen bedeutende Hürden dar, während die Entwicklung in soliden Tumorindikationen, die den größeren Markt darstellen, Sicherheitsherausforderungen mit sich bringt – was die Erkundung der TCE-Pipeline durch heimische Unternehmen erheblich erschwert.
Deshalb befinden sich viele heimische CD3-Linien hauptsächlich in frühen klinischen Phasen. Zum Beispiel ist CN201 (CD13xCD19) von ReignBio eine der schnelleren Linien, was dieses Jahr in einem präklinischen Stadium TCE-Transaktionen betrifft, aber es hat die Ib/II-Phase erreicht.
„Internationale Pharmaunternehmen wählen gerne Produkte mit ausgeprägter Effektivität oder einer soliden Basis. Doch bisher konzentrieren sich die meisten Transaktionen zwischen multinationalen Pharmakonzernen und chinesischen TCE-Assets auf die klinische IB- bis IIA-Phase, und bis zur tatsächlichen Produktion von Medikamenten ist es noch ein weiter Weg. Es ist verfrüht, durch Voranschreiten und Daten zu zeigen, welches Produkt besser ist“, meint ein Vertreter eines chinesischen Pharmaunternehmens, das BD-Transaktionen für TCE-Bi-specific Produkte anstrebt.
Anders ausgedrückt: Bis das Schicksal entschieden ist, könnte jeder das nächste "Dark Horse" werden.
Wartende Bestätigung für das neue "Trendthema" Autoimmunerkrankungen
Tatsächlich könnte jedoch der größte Einfluss auf das zukünftige Wachstum chinesischer Unternehmen, die sich mit dem TCE-Konzept befassen, nicht im aktuellen klinischen "Gewühl" von Tumoren liegen, sondern in Autoimmunerkrankungen.
Ein interessantes Phänomen ist, dass obwohl viele TCE-Linien in China Tumorindikationen untersuchen, sobald sie in einem BD-Prozess involviert sind, internationale Konzerne, die einen echten finanziellen Einsatz tätigen, tatsächlich darauf abzielen, diese auf Tumoranwendungen basierenden TCE-Linien für Autoimmunstudien zu nutzen.
Die TCE-Projekttransaktion ist die erste internationale Lizenzierung seit der Gründung des Unternehmens von Xu Yao im Januar dieses Jahres auf der J.P. Morgan Healthcare Conference (JPM) in Betracht gezogen. Damals präsentierte das Unternehmen zwar hauptsächlich Tumordaten, aber die ausländischen Pharmaunternehmen und Fonds fanden sein Potenzial für Autoimmunerkrankungen besonders attraktiv.
Kürzlich haben Candid, Ab Studio und Incyte neues Interesse an der Zusammenarbeit im Bereich Autoimmunerkrankungen geäußert. Früher hatte Candid durch die Übernahme von Vignette Bio zwei TCE-Linien erworben, die damals bereits die erste klinische Phase zur Tumorbehandlung abgeschlossen hatten. Jetzt werden sie auf die Forschung zu Autoimmunerkrankungen umgestellt und die Sicherheitsdaten werden um 2025 erwartet.
Zum einen liegt das daran, dass die Konkurrenz im TCE-Tumormarkt allmählich zunimmt, wodurch die Fähigkeit der Bi-specific Antikörper, durch T-Zellen B-Zellen abzutöten (B-Zellen spielen eine Schlüsselrolle bei Autoimmunerkrankungen, und eine tiefgreifende Entfernung von B-Zellen könnte mehreren Autoimmunerkrankungen zugutekommen), als größerer Markt für Autoimmunerkrankungen erkannt wurde. "Anders als Tumore, die einzelne Indikationen betreffen, können Autoimmunerkrankungen in viele, sogar Dutzende von Indikationen zerfallen. Gemeinsam mit dem zunehmenden Alterungstrend der Gesellschaft und der verbesserten Zahlungsstruktur in China hat Autoimmunerkrankungen ein großes Potenzial hinter sich.", so Xu Yao.
Zum anderen wurden in diesem Jahr einige reife TCE-Produkte erfolgreich an verschiedenen Autoimmunerkrankungen klinisch erprobt, was nachfolgenden Innovatoren Zuversicht verleiht.
Zum Beispiel veröffentlichte Amgen im April die Daten zur erfolgreichen Behandlung von sechs Patienten mit schwer behandelbarer rheumatoider Arthritis durch TCE-Antikörper Blinatumomab (CD19/CD3) in der Zeitschrift "Nature Medicine", womit TCE-Medikamente als eine praktikable Behandlungsmöglichkeit für rheumatoide Arthritis und andere B-Zell-vermittelte Autoimmunerkrankungen bestätigt wurden; im Juni wurden weitere therapeutische Daten für systemische Sklerose (SSc) veröffentlicht, die neben der Verbesserung der Erkrankung auch eine gute Sicherheit zeigen.
„Ein wesentlicher Punkt bei der Verwendung von TCE in autoimmune Indikationen ist die Lösung des Sicherheitsproblems, da die Sicherheitsanforderungen bei Tumoren und Immunerkrankungen sehr unterschiedlich sind. Vor 10 Jahren hätte man vielleicht gesagt, dass die Kombination von 'TCE+Autoimmun' unvorstellbar ist, da man damals noch nicht gelernt hatte, wie man die Sicherheit dieses Moleküls klinisch kontrollieren kann, um z. B. Zytokinstürme zu vermeiden. Doch durch ständige klinische Rückmeldungen, Nachverfolgung und Optimierung in diesen Jahren wurde der technische Durchbruch erzielt, und der TCE-Markt hat jetzt seinen kurz vor dem Durchbruch stehenden kritischen Punkt erreicht.“
In diesem "kritischen Punkt" haben globale Player noch keinen entscheidenden Vorsprung gezogen. Manche führende multinationale Pharmaunternehmen haben sich zwar relativ früh aufgestellt, doch befinden sich viele ihrer Projekte noch in der Anfangsphase der klinischen Phase I, wie Mosunetuzumab von Roche, das an einer systemischen Lupus-Erythematodes-Indikation arbeitet, oder IGM/Sanofis Imvotamab, das gegen rheumatoider Arthritis/systemischer Lupus erythematodes entwickelt wird.
In China befinden sich die meisten Projekte noch in der präklinischen Phase, darunter Innovatoren wie JiangsuHengrui Pharmaceuticals, SuzhouGleison Biotech und Ascentage Pharma. Unternehmen wie Shanghai Henlius, das im September 2021 die Genehmigung der Nationalen Medizinproduktebehörde für klinische Studien zu Autoimmunerkrankungen erhalten hat, stechen jedoch hervor.
In Summe befindet sich die Entwicklung von TCE-Produkten für Autoimmunerkrankungsindikationen immer noch in einem Frühstadium. Mit der klinischen Entwicklung wird der Wettbewerb unter den gegenwärtigen führenden Teilnehmern erst in einem bis zwei Jahren anfänglich entschieden werden.
Vielleicht wird der „König des Medikaments“ im TCE-Bereich unter ihnen sein.
(Xu Yao ist ein Pseudonym)
Unternehmensübersicht:
Genor Biopharma: Genor Biopharma wurde 2007 gegründet und war einst ein aufstrebendes Innovatoren im Aktienmarkt von Hongkong mit einem IPO-Ertrag von über 2,4 Milliarden Hongkong-Dollar. Vor kurzem vollzog Genor Biopharma eine umgekehrte Übernahme mit CSO-Unternehmen YTEN Pharmaceutics.
ReignBio: ReignBio wurde 2018 gegründet und ist ein von WuXi Biologics inkubiertes innovatives Pharmunternehmen. In diesem Jahr trat die TCE-Linie CN201, ein von WuXi Biologics eingeführtes Kernportfolio, dem Kooperationsprojekt mit Merck bei und wird als eine der "besten von WuXi Biologics entwickelten innovativen Portfolios" betrachtet. Finanziell erzielte ReignBio während seiner Anfänge eine Finanzierung in Höhe von 1,5 Milliarden US-Dollar, mit Investoren wie LH Merc, Boyu und Temasek.
Incyte Biopharma: Incyte Biopharma spezialisiert sich auf die Entwicklung multispezifischer Antikörper und hat die FIT-Ig® Bi-specific Antikörper-Technologieplattform mit eigenem geistigen Eigentum aufgebaut. Während des TCE-Lizenzbooms 2024, ist Incyte Biopharma eines der auffälligsten chinesischen Unternehmen, das zwei Kooperationen mit Candid eingegangen ist, wobei die zweite Transaktion die 1-Milliarden-Dollar-Marke überstieg.
Enmab Biotechnology: Enmab Biotechnology wurde 2016 gegründet und hat kürzlich eine Finanzierungsrunde unter der Leitung von Foresite Capital und dem Asia Fund von Lilly abgeschlossen. Es ist bemerkenswert, dass Foresite Capital auch einer der Hauptförderungspartner von Candid ist. Kürzlich wurde mit GSK ein Deal über TCE Drimodyne CMG1A46 im Wert von 800 Millionen Dollar abgeschlossen, bei dem sich die zukünftige Entwicklung von CMG1A46 auf Autoimmunerkrankungen wie systemischen Lupus erythematodes (SLE) und Lupusnephritis (LN) konzentrieren wird, wobei die erste klinische Phase für SLE im Jahr 2025 beginnen soll.
Vision Medicals Limited: Vision Medicals Limited wurde 2012 gegründet und beschäftigt sich seit 2020 mit der CD3 T-cell engager-Technologie. Auf der Grundlage der eigenen LeadsBody™ Forschungsplattform wurden die TCE Bi-Specific LBL-034 (GPRC5D×CD3) und LBL-033 (MUC16×CD3) entwickelt. Unter ihnen hat LBL-034 im Oktober dieses Jahres von der amerikanischen FDA eine Orphan-Drug-Bezeichnung für die Behandlung vom multiplen Myelom erhalten. Ende November reichte Vision Medicals Limited seinen Antrag an die HKEx ein.
Carnoya: Dieses an der Hongkonger Börse notierte Pharmaunternehmen verfolgt einen dualen Ansatz in Selbstimmun- und chronischen Krankheiten sowie bei Tumoren. Die in diesem Jahr vereinbarte TCE-Line CM336 ist ein BCMA/CD3 Bi-specific Antikörper, der auf der proprietären nTCE Bi-specific Antikörpertechnikplattform von Carnoya entwickelt wurde. Gegenwärtig wird eine multizentrierte, offene I/II-Phase klinische Studie zur Behandlung von refraktären oder rezidivierenden Patienten mit multiplen Myelom durchgeführt.
NonaBio: Eine Tochtergesellschaft des Biopharmaunternehmens Harbour Biomed, das als wichtiger Bestandteil von Letzterem beim Versuch angesehen wird, neue Geschäftsmodelle zu erkunden. Im ersten Halbjahr dieses Jahres beliefen sich die Servicegebühren für Beratungsdienste auf 2,326 Millionen US-Dollar, ein Anstieg von 167,4 % im Vergleich zum Vorjahr (unter Verwendung des umgerechneten Betrages von etwa 16 Millionen RMB). Außerdem hat das Unternehmen bereits mehrfach durch Lizenzverkäufe und andere Einnahmen bedeutende Einnahmen erzielt.